Vol. XXXI Issue 1
Article 2
ARTÍCULOS ORIGINALES
Análisis de genotoxicidad en eritrocitos de tortugas (Phrynops hilarii) de sitios antropizados y naturales de Entre Ríos, Argentina
Analysis of genotoxicity in erithrocytes of turtles (Phrynops hilarii) from anthropized and natural sites of Entre Ríos, Argentina
Castaño G. V.1, Cabagna Zenklusen M.2, Prieto Y.1, Manzano A. S.1
1 Centro de Investigaciones
Científicas y Transferencia de
Tecnología a la Producción
(CICYTTP-CONICET- UADER), Materi
y España, Diamante, Entre Ríos,
Argentina.
2 Universidad Nacional del Litoral,
Facultad de Bioquímica y Ciencias
Biológicas, Paraje el Pozo s/n, Santa
Fe, Argentina.
Corresponding author:
Adriana Silvina Manzano
cidmanzano@infoaire.com.ar ORCID 0000-0002-6862-857X
DOI: 10.35407/bag.2020.31.01.02
Received: 10/22/2019
Revised version received:
03/03/2020
Accepted: 03/15/2020
RESUMEN
El test de micronúcleos (MN) es un biomarcador de genotoxicidad no destructivo que permite detectar daño cromosómico y otras alteraciones nucleares (AN). Phrynops hilarii es un quelonio de agua dulce que habita regiones del centro-norte de Argentina. El objetivo principal fue determinar la presencia de MN y otras AN en eritrocitos de poblaciones naturales de P. hilarii comparando sus frecuencias entre tres sitios, dos antropizados y uno de control (ciudades de Diamante y Paraná) de Entre Ríos, Argentina, durante el periodo 2015-2016. Dieciocho individuos (seis por sitio de muestreo) fueron evaluados en los sitios: 1- PD: Parque Nacional Pre-Delta (control), 2- AG: Salto Ander Egg (agroecosistema) y 3- SU: Caleta Club Náutico (sistema urbano). Se extrajo sangre de la vena femoral. Las muestras se tiñeron con el método May Grünwald-Giemsa y se observaron bajo un microscopio con el objetivo de inmersión. Las frecuencias de micronúcleos (FMN) y alteraciones nucleares (FAN) se determinaron cada 1000 eritrocitos observados. Se encontró diferencia significativa (p<0,05) entre el sitio PD y los otros sitios (AG y SU), tanto para FMN (p=0,0021) como para FAN (p=0,0011). Los valores de las frecuencias más altos correspondieron al sitio AG (FMN: 3,33±0,62; FAN: 4,67±0,56). Finalmente, el biomonitoreo con P. hilarii fue útil, por lo que podría considerarse como especie bioindicadora para evaluar la calidad de los ambientes de Argentina.
Palabras clave: Biomarcadores de genotoxicidad; Prueba de micronúcleos; Alteraciones nucleares.
ABSTRACT
The micronucleus test (MN) is a biomarker of non-destructive genotoxicity that allows chromosomal damage and other nuclear alterations (NA) to be detected. Phrynops hilarii is a freshwater chelonium that inhabits regions of central-northern Argentina. The main objective was to determine the presence of MN and other NA in erythrocytes of natural populations of P. hilarii comparing their frequencies between three sites, two anthropized and one of control (cities of Diamante and Paraná) of Entre Ríos, Argentina, during the period 2015-2016. Eighteen individuals (six per sampling site) were evaluated at the sites: 1- PD: Pre-Delta National Park (control), 2- AG: Salto Ander Egg (agroecosystem) and 3- SU: Caleta Club Náutico (urban system). Blood was obtained from the femoral vein. The samples were stained with the May Grünwald-Giemsa method and observed under a microscope with an immersion objective. Micronucleus (MNF) and nuclear alterations (NAF) frequencies were determined every 1000 erythrocytes observed. A significant difference (p<0.05) was found between the PD site and the other sites (AG and SU), both for MNF (p=0.0021) and for NAF (p=0.0011). The highest frequency values corresponded to the AG site (MNF: 3.33 ± 0.62; NAF: 4.67 ± 0.56). Finally, biomonitoring with P. hilarii was useful, so it could be considered as a bioindicator species to assess the quality of Argentina’s environments.
Key words: Genotoxicity biomarkers; Micronucleus test; Nuclear alterations.
INTRODUCCIÓN
El test de micronúcleos (MN) es un biomarcador de
genotoxicidad no destructivo que puede aplicarse en
distintos tipos de células (epiteliales, sanguíneas,
sexuales, entre otras) y organismos (animales, vegetales
y humanos), para detectar daño cromosómico (Pastor
Benito, 2002; Poletta, 2011; Lajmanovich et al., 2012;
Caraffa et al., 2013). Este test, es un método sensible y
rápido que puede realizarse tanto en ensayos de laboratorio
como a campo, sin necesidad de sacrificar al individuo en
evaluación para la obtención de la muestra (Lajmanovich
et al., 2012; Zapata Restrepo et al., 2017). Esto es de gran
importancia, ya que puede emplearse en sucesivos
muestreos y en especies con escaso número de individuos
o en peligro de extinción (Lajmanovich et al., 2012).
Los MN son masas de cromatina con forma de pequeños
núcleos cercanos al núcleo principal en las células de la
interfase, pudiendo originarse de manera espontánea
o como respuesta a la acción de ciertos agentes (Pastor
Benito, 2002) como pueden ser los hidrocarburos
(Barsiené y Andreikénaité, 2007), metales (Paolín et al.,
2010), plaguicidas (Pastor Benito, 2002; Lajmanovich
et al., 2014), fármacos (Arranz Gutiérrez, 2016), entre
otros. Cuando esto ocurre, el material genético queda
excluido de los núcleos de las nuevas células durante la
anafase mitótica, dando lugar a formaciones redondas
en el citoplasma de la célula hija. El material genético
desprendido puede tener dos orígenes: 1- derivar de
cromosomas enteros (efecto aneugénico), donde el
daño genotóxico ha afectado a proteínas del cinetocoro,
al centrómero o al huso mitótico, generando un retraso
mitótico y un desequilibrio en la distribución de los
cromosomas, 2- pueden formarse de fragmentos
cromosómicos acéntricos que han sido excluidos de
los núcleos de las nuevas células (efecto clastogénico)
durante la anafase mitótica (Cabagna Zenklusen, 2012).
Numerosos trabajos en fauna han aplicado el test de
MN en eritrocitos, para evaluar a través de su frecuencia
(FMN) los efectos provocados por distintos agentes en
el material genético y en la división celular (Pollo et
al., 2012; Caraffa et al., 2013; Latorre et al., 2015). Para
determinar el potencial de una especie como organismo
bioindicador o centinela se utiliza como valor referencia
la frecuencia basal de micronúcleos (FBMN). Este
valor refiere al número de MN provocados de manera
espontánea como resultado de procesos normales de
replicación y/o división celular (Cabagna Zenklusen,
2012; Latorre et al., 2015).
Otras alteraciones nucleares (AN) pueden analizarse
al aplicar el test de MN y son utilizadas como un
complemento, ya que en varios estudios fueron
señaladas como respuesta a la acción de determinados
agentes tóxicos (Ayllon y García Vázquez, 2000;
Cabagna Zenklusen, 2012; Hayretdağ et al., 2014;
Hernández Guzmán et al., 2015). Se consideran como
AN las siguientes características descriptas por Carrasco
et al. (1990): 1- núcleo escotado (KN): invaginación
relativamente pequeña en la membrana nuclear y
cromatina no condensada; 2- núcleo mellado (EN):
presencia de una muesca en el núcleo; 3- lóbulo o brote
nuclear (LN): morfología semejante a un MN conectado
o unido al núcleo; 4- célula binucleada (BN): célula
con presencia de dos núcleos de tamaños semejantes o
similares. El mecanismo por el cual se producen las AN
no es conocido con claridad. López González et al. (2017)
mencionaron que cuando la célula detecta una región
de ácido desoxirribonucleico (ADN) afectada, se inicia
un proceso de reparación y eliminación de la cromatina.
La región alterada se mueve a la periferia del núcleo y
se elimina por exocitosis. Antes de que el proceso de
reparación y eliminación de la cromatina culmine, la
membrana nuclear presenta algunas imperfecciones,
ocasionando AN.
Los agentes genotóxicos son sustancias que pueden
actuar de forma directa o indirecta sobre el material
genético (ADN) y provocar efectos a concentraciones
subletales (Gutiérrez, 2013). Estos agentes pueden ser
liberados al ambiente por distintas actividades humanas,
ya sean productivas como la minería, la agricultura y
distintos procesos industriales o por actividades urbanas
como el vertido de efluentes cloacales, emisiones
vehiculares, aguas residuales hospitalarias y de
estaciones de combustible, entre otras (Paz et al., 2008;
Zuluaga Quintero et al., 2009; Gutiérrez, 2013; González
Torres et al., 2015). Para evaluar el riesgo potencial de
poblaciones naturales expuestas a agentes genotóxicos,
son utilizadas especies indicadoras o centinelas y
distintos biomarcadores, ya que suministran señales de
alarma temprana ante la presencia a tóxicos (Cabagna
Zenklusen, 2012; Caraffa et al., 2013).
Los reptiles son organismos muy sensibles a cambios
en las condiciones del ambiente, por lo que en muchos
casos fueron utilizados como indicadores o centinelas de
contaminación, debido a que presentan características
como: poblaciones persistentes en diferentes hábitats
(acuáticos y terrestres), longevidad, posición alta en la
cadena alimentaria, alta sensibilidad a contaminantes,
amplia distribución geográfica y fidelidad al sitio
(Gardner y Oberdorster, 2005; Poletta et al., 2008;
Poletta et al., 2013). Dentro de estos, las tortugas han
sido propuestas como organismos bioindicadores y/o
centinelas para evaluar su exposición a sustancias
tóxicas (Andreani et al., 2007; De Solla et al, 2007; De
Solla et al., 2008; Latorre et al., 2015).
Phrynops hilarii es un quelonio de agua dulce
perteneciente al orden Testudines, suborden Pleurodira
y familia Chelidae. La distribución geográfica de la
especie abarca algunas regiones de Sudamérica (Latorre
et al., 2015).
Particularmente en Argentina se la puede encontrar
en áreas de la región centro-norte del país entre las
provincias de Buenos Aires, Entre Ríos, Corrientes,
Santa Fe, Córdoba, Misiones, Chaco, Formosa, Santiago
del Estero y Mendoza (Derocco et al., 2005). Las áreas
que habita pueden presentar distintas condiciones
topográficas, fisicoquímicas, entre otras, como lagunas,
esteros, arroyos lentos, ríos, cursos fluviales con
lecho de fango o arena y bañados asociados a juncos y
vegetación flotante; además, se la puede encontrar en
áreas antropizadas como arrozales, cuneta al borde de
campos cultivados y tajamares, en los cuales se encuentra
especialmente expuesta a sustancias tóxicas (Cei, 1993;
Cabrera, 1998; Richard y Waller, 2000; Carreira et al.,
2005; Tortato, 2007).
Los estudios de genotoxicidad basados en la aplicación
del test de MN y la evaluación de otras AN en reptiles de
Argentina, son recientes (Poletta et al., 2008; Poletta et
al., 2009; Poletta, 2011; Shaumburg et al., 2012; López
González et al., 2013; Shaumburg et al., 2014; Shaumburg
et al., 2016; López González et al., 2017). En lo que
respecta a tortugas de nuestro país, los datos hallados
son escasos y acotados a la descripción de la FBMN y a
la FMN en P. hilarii y Trachemys dorbigni en condiciones
de cautiverio, sin indagar en la descripción de otras
AN (Boned et al., 2011; López González et al., 2012;
Latorre et al., 2015). El objetivo principal de este trabajo
fue determinar la presencia de MN y otras AN en los
eritrocitos de poblaciones naturales de Phrynops hilarii comparando sus frecuencias entre sitios antropizados y
control (en las ciudades de Diamante y Paraná) de Entre
Ríos, Argentina.
MATERIALES Y MÉTODOS
Área de estudio y sitios de muestreo
El estudio se realizó en un área comprendida entre los
departamentos Diamante y Paraná de la provincia de
Entre Ríos, Argentina. Los sitios seleccionados fueron
dos zonas antropizadas y una de control: 1- PD: Parque
Nacional Pre-Delta (control, 32° 03’ 43” S y 60° 38’ 39”
O), 2- AG: Salto Ander Egg (agroecosistema, 32° 07’
42.64’’ S y 60° 25.40’ 13” O) y 3- SU: Caleta Club Náutico
(sistema urbano, 31°42’ 55” S y 60° 30’ 17” O), durante
los meses cálidos (Octubre-Marzo) de los años 2015 y
2016 (Figura 1). Los sitios pertenecen a la ecorregión
Delta e Islas del Paraná y Espinal (Burkart et al., 1999),
con temperaturas medias anuales inferiores a los 20°C y
las precipitaciones medias anuales abarcan un periodo
de mayor frecuencia entre los meses de octubre-abril
(73% del total anual), sin embargo, en los meses de
verano pueden presentarse lapsos de déficit hídrico
(Rojas y Saluso, 1987). El uso intensivo de la tierra en
estas regiones, le da al paisaje un perfil muy antrópico,
debido a que se encuentra principalmente ocupado por
superficies agrícolas, pasturas implantadas y en menor
medida, por pasturas y bosques naturales, así como
también, por áreas industriales y urbanas, con sitios
de parches dispersos de bosques nativos (Aceñolaza y
Rodríguez, 2013).
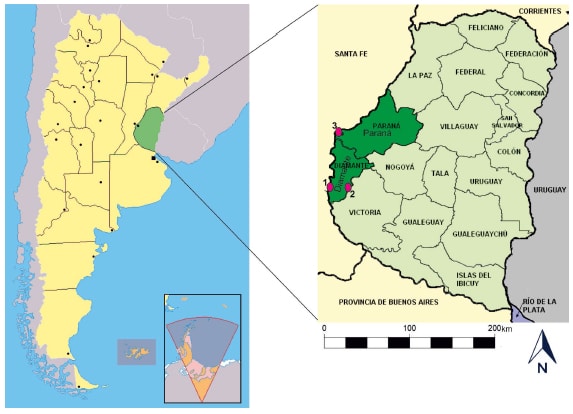
Figura 1. Área de estudio y sitios de muestreo. 1-Parque Nacional Pre Delta (sitio control). 2-Salto Ander Egg (sitio agroecosistema). 3-Caleta Club
Náutico (sitio urbano).
Captura de individuos y extracción de sangre
Se capturaron 18 individuos (seis por sitio de muestreo)
con trampas tipo embudo (Aguirre León, 2011) a las que
se les agregó cebos atrayentes (trozos de peces). De cada
individuo se registró el largo curvilíneo del caparazón
(LC, mm) con un centímetro de 1mm de precisión. El
peso corporal (MC, kg) de los individuos se registró con
balanza manual electrónica con 0,01 kg de precisión. Los
animales fueron marcados en el borde de su caparazón
mediante la realización de una pequeña muesca con
sierra manual para el control de recapturas.
La extracción de sangre se realizó de la vena femoral
con jeringas estériles de 1ml previamente heparinizadas
(anticoagulante) y aguja TERUMO® 25G 0.5mm, sin
anestésicos para evitar la alteración de los componentes
de la sangre (Duguy, 1982; Troiano y Silva, 1998;
Attademo et al., 2012). Todos los animales luego de la
extracción fueron reincorporados a su lugar. Las muestras
fueron llevadas refrigeradas al Laboratorio de Muestras
Biológicas del Centro de Investigaciones Científicas y
Transferencia de Tecnología a la Producción (CICYTTPCONICET)
de la cuidad de Diamante, Entre Ríos, para
su posterior procesamiento. Para las actividades y
manipulación de los animales se siguieron los Principios
Éticos para la Investigación en el Laboratorio, Granja
y Animales Silvestres (REFBR-CONICET, 2005), y se
contaron con los permisos correspondientes de la
Dirección Recursos Naturales de la provincia de Entre
Ríos (Resolución Nº1721) y de la Administración de
Parque Nacionales (Nº CRCE 6).
Test de micronúcleos
Para la evaluación de MN y otras AN a través del test de
MN, se prepararon extendidos sanguíneos de cada uno
de los individuos en portaobjetos limpios y secados
al aire. Posteriormente se tiñeron con solución May
Grünwald-Giemsa y se observaron en un microscopio
Carl Zeiss Axiostar con objetivo de inmersión.
Para el conteo de MN se seleccionaron los eritrocitos
intactos y se reconocieron siguiendo los criterios
descriptos por Fenech (2000), donde señala que el
diámetro del MN no debe superar el 1/6 o 1/3 del tamaño
del núcleo principal y debe estar separado de este y
presentar una morfología, coloración e intensidad
similar a la del núcleo principal.
Para determinar la FMN de las muestras por sitio, se
realizó el conteo de la cantidad de células que presentaron
MN en 1000 eritrocitos observados por frotis de cada
individuo (López González et al., 2017).
La FAN total se obtuvo sumando todas las AN que se
observaron en las muestras de los seis individuos de
cada área y se expresaron cada 1000 eritrocitos contados
por individuo por sitio (Cabagna Zenklusen et al., 2011).
Análisis estadístico
Los datos descriptivos de los individuos a los que se
extrajeron las muestras son: media ± error estándar
(EE) y tamaño de la muestra (n). Los datos fueron
testeados en cuanto a su normalidad (Shapiro-
Wilks) y homocedasticidad (test de Levene). Para las
comparaciones de medias se utilizó el test no paramétrico
Kruskal Wallis (p<0,05). Todos los análisis estadísticos
fueron realizados con el software estadístico INFOSTAT
versión 2012 profesional (Di Rienzo et al., 2012).
RESULTADOS
En la Tabla 1 se consignan los valores de los parámetros biológicos determinados en los individuos analizados de cada sitio. En los extendidos sanguíneos analizados se distinguieron tres tipos de AN: eritrocito con brote nuclear (LN), eritrocito con núcleo mellado (EN) y eritrocito con micronúcleo (MN) (Figura 2).
Tabla 1. Parámetros biológicos de P. hilarii, peso corporal (MC) y longitud
caparazón (LC). Sitios: control (PD), agroecosistema (AG) y sistema
urbano (SU). n: tamaño de la muestra. Los valores se expresaron como
media ± EE.
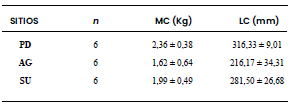
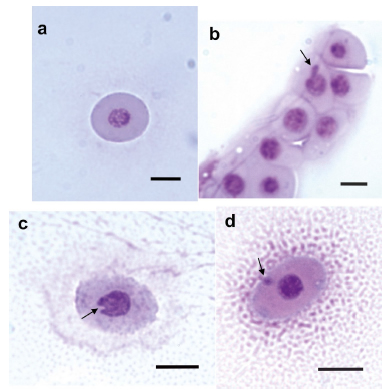
Figura 2. Eritrocitos de Phrynops hilarii: a) normal; b) eritrocito con brote; c) eritrocito con
núcleo mellado; d) eritrocito con micronúcleo. Escala: 5μm.
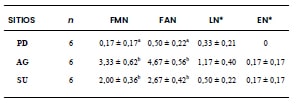
En la Tabla 2 se exponen los valores de la FMN, FAN, LN y EN de los sitios muestreados. En el sitio control (PD), los datos corresponden a los resultados basales de las frecuencias en este sitio. Se observaron diferencias significativas (p<0,05) entre el sitio PD y los otros sitios (AG y SU), tanto para la FMN (p= 0,0021) como para la FAN (p=0,0011), mientras que para los demás parámetros celulares (LN y EN) no se encontraron diferencias significativas (p>0,05) entre los sitios. Entre las áreas antropizadas, los mayores registros de las frecuencias correspondieron al sitio AG. Además, no se encontró correlación entre los parámetros biológicos (MC y LC de P. hilarii) y las frecuencias de MN y de AN de los sitios AG (MC-FMN: r2= 0,62 y LC-FMN: r2= 0,31; MC-FAN: r2= 0,24 y LC-FAN: r2-0,24), SU (MCFMN: r2= -0,72 y LC-FMN: r2= -0,60; FAN-MC: r2= -0,03 y FAN-LC: r2= 0,09) y PD (FMN-MC: r2= 0,13 y FMN-LC: r2= -0,39; FAN-MC: r2= 0,29 y FAN-LC: r2= 0,10).
Tabla 2. Parámetros celulares evaluados en P. hilarii. FMN: frecuencia
de micronúcleos; FAN: frecuencia de alteraciones nucleares; LN: lóbulo
nuclear; EN: núcleo mellado; en 1000 eritrocitos contados por muestra.
Sitios: control (PD), agroecosistema (AG) y sistema urbano (SU). n:
tamaño de la muestra. Todos los valores se expresaron como media ±
EE. Superíndices a y b en las columnas señalan diferencias significativas
entre los sitios (p<0,05). (*) Sin diferencias significativas.
DISCUSIÓN
Actualmente existe un gran interés en estudios
ecotoxicológicos con reptiles, debido a que las
características fisiológicas y ecológicas que presentan,
permiten evaluar el estado de contaminación de un
ambiente (Quiróz Herrera y Palacio Baena, 2017).
Varios autores han aplicado el test de MN (Zúñiga
González et al., 2000; 2001; Poletta, 2011; Shaumburg
et al., 2012; 2014; Zapata et al., 2016; López González et
al., 2017), y de otras AN (Strunjak Perovic et al., 2010;
Hayretdağ et al., 2014; Hernández Guzmán et al., 2015;
López González et al., 2017) en caimanes, serpientes y en
otras especies de tortugas.
Los resultados de la FMN obtenidos del sitio PD
(control) del presente trabajo fueron tomados como
valores basales, al igual que la FAN para dicho sitio,
debido a que no hay antecedentes hasta el momento de
valores basales en individuos de P. hilarii en la naturaleza
(Tabla 2). Los datos de FBMN obtenidos, fueron menores
en comparación con los reportados por los autores
Boned et al. (2011) y Latorre et al. (2015) para individuos
de esta especie en condiciones de cautiverio. Asimismo,
se encontró en el trabajo de Zapata et al. (2016) que la
FBMN obtenida de individuos de Trachemys callirostris
expuestos a las actividades agrícolas, industriales y
mineras fue mayor que el resultado obtenido en el
presente estudio; de igual manera ocurrió en el trabajo
de Da Silva Silveira (2016), en el cual la FBMN obtenida
de las especies: Chelonia mydas, Caretta caretta y un
híbrido entre las especies C. caretta y Lepidochelys olivácea
de áreas expuestas a descargas de contaminantes de
residuos sólidos y metales pesados fueron mayores a las
del presente trabajo.
Por otra parte, Zúñiga González et al. (2000; 2001)
informaron valores de la FBMN para varias especies de
vertebrados tanto en la naturaleza como en cautiverio,
en el cual, detallaron datos para dos especies de tortugas
de agua dulce Macroclemys temminckii y Kinosternon
subrubrum, cuyos valores reportados fueron nulos,
pudiendo deberse estos resultados al bajo número de
individuos analizados, ya que los autores utilizaron un
individuo de la primera especie mencionada y dos de la
segunda (Poletta, 2011).
En lo que respecta a la FBAN, los datos obtenidos en
el presente trabajo son los primeros en tortugas P. hilarii
de poblaciones naturales, ya que solamente se encontró
en la bibliografía el trabajo de Da Silva Silveira (2016), en
el cual describe eritrocitos con brotes además de los MN
en las especies anteriormente mencionadas (C. mydas, C.
caretta y un híbrido entre C. caretta y L. olivácea).
Los autores Matson et al. (2005) determinaron la FMN
en las tortugas Emys orbicularis expuestas a descargas
industriales y Borrat et al. (2011) en la especie C. mydas
expuesta a las actividades agrícolas, y Quiroz Herrera
y Palacio Baena (2017) en L. olivácea para determinar
efectos genotóxicos de contaminantes en una zona
expuesta a los agroquímicos y metales pesados.
Las FMN obtenidas de las tortugas de los trabajos
de Matson et al. (2005) y Borrat et al. (2011), fueron
superiores a los valores obtenidos de los sitios
antropizados (AG y SU).
No obstante, en el estudio de
Quiroz Herrera y Palacio Baena (2017), los resultados de
sus análisis fueron bajos en relación a los valores de los
sitios AG y SU.
Finalmente, las muestras analizadas de P. hilarii del
sitio PD tuvieron escasas AN, lo cual, podría asociarse a
eventos espontáneos (Cabagna Zenklusen, 2012), ya que
las tortugas capturadas en esta área (Parque Nacional),
corresponden a un sitio protegido, relativamente alejado
de campos agrícolas e industrias.
El aumento de las frecuencias de MN y AN observadas
en P. hilarii de los sitios AG y SU, podrían estar asociadas
fuertemente a las actividades náuticas y agrícolas,
produciendo un incremento de las alteraciones con
respecto a las frecuencias obtenidas en el sitio PD.
Estos resultados, coinciden con algunos de los trabajos
anteriormente mencionados, como los de Matson et
al. (2005), Hayretdağ et al. (2014) y López González et
al. (2017), ya que en los mismos, los sitios utilizados
en sus estudios, expuestos a contaminantes o ensayos
de laboratorio por inducción a tóxicos, produjeron un
aumento en las frecuencias de MN y AN con respecto a
sus controles.
De acuerdo a los resultados obtenidos en el presente
trabajo, consideramos que el biomonitoreo realizado
con P. hilarii fue útil, por lo que podría ser utilizada
como especie bioindicadora para evaluar calidad de los
ambientes de Argentina. Si bien el número de individuos
analizados fue bajo, cabe resaltar que estos animales
se encontraban en libertad, expuestos naturalmente
a las condiciones de los ambientes que habitan. En
este contexto, este trabajo es el primero de este tipo,
y consideramos que ampliar el número de individuos
y sitios de estudio podría incrementar el valor de los
resultados hallados, y es un desafío que nos planteamos
para futuros trabajos en el área de estudio.
AGRADECIMIENTOS
Agradecemos al CICYTTP-CONICET por los materiales otorgados y el espacio brindado para la realización de las actividades en el laboratorio de herpetología; a la Administración de Parques Nacionales y a la Secretaría de Medio Ambiente de la provincia de Entre Ríos por los permisos otorgados; a Silvia Etcheverry por el apoyo en el laboratorio; a Estefanía Reyes por la ayuda brindada en los muestreos; y a Agustín Bassó por la explicación en la toma de muestras de sangre. Este trabajo fue realizado en parte con financiamiento de PICT 2016-2772 y PIP 389.
BIBLIOGRAFÍA
1. Aceñolaza P.G., Rodríguez E.E. (2013) Humedales de los tributarios cortos del río Paraná. En: Benzaquén L., Blanco D., Bó R., Kandus P., Lingua G., Minotti P., Quintana R.D., Sverlij S., Vidal L. (Eds.) Inventario de los humedales de Argentina: sistemas de paisajes de humedales del corredor fluvial Paraná-Paraguay. Buenos Aires, Argentina. pp. 245-252.
2. Aguirre León G. (2011) Métodos de estimación, captura y contención de anfibios y reptiles. En: Gallina S., López González C. (Eds.) Manual de técnicas para el estudio de la fauna. Volumen I. Universidad Autónoma de Querétaro-Instituto de Ecología, A.C. Querétaro, México, pp. 61-85.
3. Andreani G., Santoro M., Cottignoloc S., Fabbri M., Carpené E., Elsani G. (2007) Metal distribution and metallothionein in loggerhead (Caretta caretta) and green (Chelonia mydas) sea turtles. Sci Total Environ. 390 (1): 287-294
4. Arranz Gutiérrez P. (2016) Evaluación de la posible capacidad genotóxica de fármacos antihipertensivos: losartán e irbesartán. Tesis de Grado, Universidad del País Vasco.
5. Attademo A.M., Lajmanovich R.C., Peltzer P.M., Bassó A., Junges C., Cabagna Zenklusen M. (2012) Plasma b-esterease and glutathione s-transferase activities in the South American reptiles Caiman latirostris (Crocodylia, Alligatoridae) and Phrynops hilarii (Testudines, Chelidae).Water Air Soil Pollut.223 (6): 3321-3331
6. Ayllon F., García Vázquez E. (2000) Induction of micronuclei and other nuclear abnormalities in European mirrow Phoxinus phoxinus and mollie Poecilia latipinna: an assessment of the fish micronucleus test. Mutat. Res. 467: 177-186
7. Barsiené J., Antdreikénaité L. (2007) Induction of micronuclei and other nuclear abnormalities in blue mussels exposed to crude oil from the North Sea. Ekologija. 53:9-15
8. Boned M.J., López González E., Latorre M.A., Poletta G.L., Siroski P.A. (2011) Determinación del valor basal de micronúcleos (MN) en la tortuga de laguna (Phrynops hilarii). J. Basic Appl. Genet. 40: 91
9. Borrat V., Villar S., Marquez A., Martinez Souza G., Fallabrino A., Novello A. (2011) Evaluación del estado de la tortuga verde (Chelonia mydas) mediante el uso de biomarcadores de genotoxicidad en el área protegida “Cerro verde e islas de La Coronilla” próximas al canal Andreoni. V Jornada sobre Tartarugas Marinhas do Atlântico Sul Ocidental 27-28 de Noviembre de 2011, Florianópolis, Brasil; pp. 88-92.
10. Burkart R., Barbaro N.O., Sánchez R.O., Gómez D.A. (1999) Eco-regiones de la Argentina. Ed. PRODIA. Buenos Aires, Argentina.
11. Cabagna Zenklusen M.C. (2012) Caracterización hematológica de especies de anfibios anuros con distribución en los ecosistemas del litoral fluvial argentino (provincias de Entre Ríos y Santa Fe). Potencialidad de su utilización como biomarcadores. Tesis Doctoral, Universidad Nacional del Litoral, Facultad de Bioquímica y Ciencias Biológicas, Santa Fe, Argentina.
12. Cabagna Zenklusen M.C., Lajmanovich C.R., Attademo A.M., Peltzer P.M., Junges C.M., Fiorenza Biancucci G., Bassó A. (2011) Hematología y citoquímica de las células sanguíneas de Rhinella fernandezae (Anura: Bufonidae) en Espinal y Delta-Islas del río Paraná, Argentina. Rev. Biol. Trop.59 (1): 17-28
13. Cabrera R.M. (1998) Las tortugas continentales de Sudamérica austral. Talleres gráficos BR Copias, Córdoba, Argentina.
14. Caraffa E., Bionda C., Pollo F.E., Salas N.E., Martino A.L. (2013) Determinación de la frecuencia de micronúcleos en eritrocitos de Bufo arenarum que habitan ambientes urbanizados. Acta Toxicol. Argent. 21(2): 78-84
15. Carrasco K.R., Tilbury K.L., Mayers M.S. (1990) Assessment of the piscine micronuclei test as an in-situ biological indicator of chemical contaminants effects. Can. J. Fish Aquat. Sci. 47: 2123-2136
16. Carreira Vidal S., Meneghel M., Achaval F. (2005) Notas descriptivas y biológicas. En: Elbert L. (Ed.) Reptiles de Uruguay. Universidad de la República, Facultad de Ciencias, Montevideo, Uruguay, pp. 97-100.
17. Cei J.M. (1993) Reptiles del noroeste, nordeste y este de Argentina. Herpetofauna de las selvas subtropicales, puna y pampas. Museo Regionale di Scienze Naturali di Torino, Monografia XIV, Torino.
18. Da Silva Silveira E. (2016) Avaliação dos danos mutagênicos através da análise de micronúcleos em eritrócitos de tartarugas marinhas no Litoral Norte e Médio Leste do Rio Grande do Sul, Brasil. Monografía, Universidad Estatal de Rio Grande do Sul, en convenio con la Universidad Federal de Rio Grande do Sul, Brasil.
19. De Solla R., Fernie K.J., Letcher S.G., Chu K.G., Drovillard K.G., Shahmiri S. (2007) Snapping turtles (Chelydra serpentina) as bioindicators in canadian areas of concern in the great lakes basin. 1. Polybrominated diphenyl ethers, polychlorinated biphenyls, and organochlorine pesticides in eggs. Rev. Environ. Sci. Technol. 41(21): 7252-7259
20. De Solla S.R., Fernie K.J., Asphole S. (2008) Snapping turtles (Chelydra serpentina) as bioindicators in canadian areas of concern in the great lakes basin. II. Changes in hatching success and hatchling deformities in relation to persistent organic pollutants. Rev. Environ. Pollut. 153: 529-536
21. Derocco N.N., Alcalde L., Rosset S.D. (2005) Ampliación de la distribución de Phrynops hilarii (Pleurodira: Chelidae) en Argentina. Cuad. herpetol. 19 (1): 63
22. Di Rienzo J.A., Casanoves F., Balzarini M.G., González L., Tablada M., Robledo C.W. (2012) Grupo InfoStat, FCA, Universidad Nacional de Córdoba, Argentina. URL http://www.infostat.com.ar
23. Duguy R. (1982) Biology of the Reptilian. Vol. III. New York. Carl Gans (Ed.) Academic Press. New York, pp. 155-188
24. Fenech M. (2000) The in vitro micronucleus technique. Mutat. Res.455:81-95
25. Gardner S.C., Oberdorster E. (2005) Toxicology of Reptiles. New perspectives: Toxicology and the Environment. Editorial Taylor & Francis Group, Boca Raton, Florida, EE.UU.
26. González Torres H., Moreno Rossi A., Quintana Sosa M. (2015) Efecto genotóxico de mezclas complejas de hidrocarburos en trabajadores de estaciones de servicio de gasolina. Salud Uninorte.31: 91-100
27. Gutiérrez J. M. (2013) Micronúcleos en peces como indicadores de calidad ambiental en estuarios de la costa uruguaya. Tesis de Pre Grado, Universidad de la República Uruguay, Facultad de Ciencias, Montevideo, Uruguay.
28. Hayretdağ S., Gürkan M., Yakin B.Y., Tok C.V. (2014) A preliminary study on micronuclei and nuclear abnormalities in the erythrocytes of some Colubrid snakes from Turkey. Biharean Biol. 8 (1): 53-55
29. Hernández Guzmán J., Arias Trinidad A., Islas Jesús R.I., Fraire Vázquez A., De La Cruz Izquierdo R.I., García Guzmán N.C., Ruíz X. (2015) Cromosomas, lesión del ADN y malformación nuclear en la tortuga dulceacuícola (Testudines: Kinosternidae). The Biolog. 13 (2): 201-211
30. Lajmanovich R.C., Peltzer P.M., Attademo A.M., Cabagna Zenklusen M.C., Junges C.M. (2012) Los agroquímicos y su impacto en los anfibios: un dilema de difícil solución. Rev. Quím.Viva.3: 184-198
31. Lajmanovich R.C., Cabagna Zenklusen M.C., Attademo A.M., Junges C.M., Peltzer P.M., Bassó A., Lorenzatti E. (2014) Induction of micronuclei and nuclear abnormalities in tadpoles of the common toad (Rhinella arenarum) treated with the herbicides Liberty® and Glufosinate-ammonium. Mutat. Res. 769: 7-12
32. Latorre M.A., López González E., Siroski P.A., Poletta G.L. (2015) Basal frequency of micronuclei and hematological parameters in the side-necked turtle (Phrynops hilarii). Acta Herpetol. 9 (2): 1827-9635
33. López González E.C., Latorre M.A., Boned M.J., Poletta G.L., Siroski P. (2012) Determinación de la frecuencia de micronúcleos en dos especies de tortugas acuáticas: (Phrynops hilarii) y tortuga pintada (Trachemys dorbigni). IV Congreso Argentino de la Sociedad de Toxicología y Química Ambiental SETAC Argentina.
34. López González E.C, Latorre M.A., Larriera A., Siroski P.A., Poletta G.L. (2013) Induction of micronuclei in broad snouted caiman (Caiman latirostris) hatchlings exposed in vivo to Roundup® (glyphosate) concentrations used in agriculture. Pestic. Biochem. Physiol. 105: 131-134
35. López González E.C., Larriera A., Siroski P.A., Poletta G.L. (2017) Micronuclei and other nuclear abnormalities on Caiman latirostris (Broad snouted caiman) hatchlings after embryonic exposure to different pesticide formulations. Ecotoxicol. Environ. Saf. 136: 84-91
36. Matson C.W., Palatnikov G., Izlamzadeh A., Mc Donald T.J., Autenrieth R.L., Donnelly K.C., Bickham J.W. (2005) Chromosomal damage in two Species of aquatic turtles (Emys orbicularis and Mauremys caspica) inhabiting contaminated sites in Azerbaijan. Ecotoxicol. 14: 1-13
37. Paolín R., Cáceres V., Tello A.V., Torres G.A. (2010) Uso de biomarcadores genotóxicos e histopatológicos para evaluar el efecto de metales en tilapia (Oreochromis niloticus L.L) presente en la laguna el Sonso (Valle de Cauca). Rev. Asoc. Col. Cienc. 22: 109-121
38. Pastor Benito S. (2002) Biomonitorización citogenética de cuatro poblaciones agrícolas europeas, expuestas a plaguicidas, mediante el ensayo de micronúcleos. Tesis Doctoral, Universidad Autónoma de Barcelona, Facultad de Ciencias, Departamento de Genética y Microbiología, Barcelona, España.
39. Paz M., Magdaleno A., Balbis N., Morehon J. (2008) Genotoxicidad y determinación de compuestos tóxicos en un residuo líquido hospitalario de Buenos Aires, Argentina. Int. Contam. Ambient. 24 (2): 79-87
40. Poletta G.L., Larriera A., Kleinsorge E., Mudry M.D. (2008) Caiman latirostris (broadsnouted caiman) as a sentinel organism for genotoxic monitoring: Basal values determination of Micronucleus and Comet assay. Mutat. Res. 650: 202–209
41. Poletta G. L., Larriera A., Kleinsorge E., Mudry M.D. (2009) Genotoxicity of the herbicide formulation Roundup (glyphosate) in broad-snouted caimán (Caiman latirostris) evidenced by the comet assay and the micronucleus test. Mutat. Res. 672: 95-102
42. Poletta G.L. (2011) Monitoreo de daño inducido por plaguicidas en Caimán latirostris (Yacaré overo) como organismo centinela de los humedales de Argentina. Tesis Doctoral, Universidad de Buenos Aires, Facultad de Ciencias Exactas y Naturales. Buenos Aires, Argentina.
43. Poletta G.L, Siroski P.A, Amavet P.S, Ortega H.H, Mudry M.D. (2013) Reptiles as animal models: examples or their utility in genetics, immunology and toxicology. En: Lutterschmidt, W (Ed.) Reptiles in Research: Investigations of Ecology, Physiology and Behavior from Desert to Sea, Nova Science Publishers, New York, USA, pp. 407-445.
44. Pollo F.E., Salas N.E., Mancini M.A., Martino A.L. (2012) Estudio comparativo de la frecuencia de micronúcleos y anormalidades nucleares en eritrocitos de tres especies ícticas. Acta Toxicol. Argent. 20 (2): 62-67
45. Quiroz Herrera V.H., Palacio Baena J. (2017) Niveles sanguíneos de biomarcadores de daño genético en eritrocitos de Lepidochelys olivacea (Cheloniidae) en Colombia. Acta Biol. Colomb. 22 (3): 322-330
46. Reference Ethical Framework for Biomedics Research (REFBR) (2005). Res. N°1047 Anexo II. Ethical principles for research with laboratory, farm and wild animals. CONICET, Buenos Aires, Argentina.
47. Richard E., Waller T. (2000) Categorización de las tortugas de Argentina. En Lavilla E.O., Richard E. y Scrocchi G. (Eds.). Categorización de los Anfibios y Reptiles de Argentina. Asociación Herpetológica Argentina, Buenos Aires, Argentina pp. 35-44.
48. Rojas A.E.C., Saluso J.R. (1987) Informe Climático de la Provincia de Entre Ríos. Publicación Técnica Nº 14. Estación Experimental Agropecuaria Paraná - Instituto Nacional de Tecnología Agropecuaria (EEA-INTA), Paraná, Entre Ríos, Argentina.
49. Shaumburg L.G., Poletta G.L., Siroski P.A., Mudry M.D. (2012) Baseline values of Micronuclei and Comet Assay in the lizard Tupinambis merianae (Teiidae, Squamata). Ecotoxicol. Environ. Saf. 84: 99-103
50. Shaumburg L.G., Poletta G.L., Siroski P.A., Mudry M.D. (2014) Spontaneous genetic damage in the tegu lizard (Tupinambis merianae): The effect of age. Mutat. Res.766: 5-9
51. Shaumburg L.G., Siroski P.A., Poletta G.L., Mudry M.D. (2016) Genotoxicity induced by Roundup® (Glyphosate) in tegu lizard (Salvator merianae) embryos. Pestic. Biochem. Physiol.130.71-78
52. Strunjak Perovic I., Lisicic D., Coz Rakovak R., Topic Popovic N., Jardan M., Benkovic V., Tadic Z. (2010) Evaluation of micronucleus and erythrocytic nuclear abnormalities in Balkan whip snake Hierophis gemonensis. Ecotoxicol.19: 1460–1465
53. Tortato M.A. (2007) Contribuição ao conhecimento de Phrynops hilarii (Duméril & Bibron, 1835) (Testudines, Chelidae) em área de restinga no Estado de Santa Catarina, Sul do Brasil. Biotemas. 20 (1): 119-122.
54. Troiano J.C., Silva M.C. (1998) Valores hematológicos de referencia en tortuga terrestre argentina (Chelonoidis chilensis chilensis). Analect. Vet. (18): 47-51
55. Zapata L.M., Bock B.C., Orozco L.Y., Palacio J.A. (2016) Application of the micronucleus test and comet assay in Trachemys callirostris erythrocytes as a model for in situ genotoxic monitoring. Ecotoxicol. Environ. Saf. 127: 108-116
56. Zapata Restrepo L.M., Orozco Jiménez L.Y., Rueda Cardona M., Echavarría S.L., Mena Moreno N., Palacio Baena J.A. (2017) Evaluación genotóxica del agua del Río Grande (Antioquia, Colombia) mediante frecuencia de eritrocitos micronucleados de Brycon henni (Characiformes: Characidae). Rev Biol Trop 65: 405-414.
57. Zuluaga Quintero M., Valencia Ruíz A. M., Ortíz Trujillo I. C. (2009) Efecto genotóxico de contaminantes atmosféricos. Medicina UPB. 28: 33-41
58. Zúñiga González G., Torres Bugarín O., Luna Aguirre J., González Rodríguez A., Zamora Pérez A., Gómez Meda B.C., Ventura Aguilar A.J., Ramos Ibarra M.L., Ramos Mora A., Ortiz G.G., Gallego Arreola M.P. (2000) Spontaneous micronuclei in peripheral blood erythrocytes from 54 animal species mammals, reptiles and birds: Part two. Mutat. Res.467: 99-103
59. Zúñiga González G., Torres Bugarín O., Zamora Pérez A., Gómez Meda B.C., Ramos Ibarra M.L., Martínez González S., González Rodríguez A., Luna Aguirre J., Ramos Mora A., Oliveros Lira D., Gallegos Arreola M. P. (2001) Differences in the number of micronucleated erythrocytes among young and adult animals including humans: Spontaneous micronuclei in 43 species. Toxicol. Environ. Mutag.494: 161–167



